

Pure 制备色谱
在微生物次级代谢产物中的应用
Pure 应用
”
1
简介
反向柱层析法(Reverse Phase Column Chromatography, RPCC)是天然产物分离的重要手段之一,其核心作用是通过极性差异实现复杂混合物中目标成分的纯化,固定相为非极性(C18、C8 键合硅胶),流动相为极性溶剂(水、甲醇、乙腈等)。极性越弱的成分与固定相作用越强,洗脱越慢,从而实现分离。
本实验通过制备型快速柱层析技术将正相柱层析组分按照极性大小洗脱,流动相为甲醇、水,极性大的组分先被洗脱下来,极性小的组分后被洗脱下来,将洗脱下来的组分减压旋干称重,利用高效液相色谱查看分离效果。

▲ 图1:Buchi Pure C-810 纯化分离系统
2
实验
2.1 设备
Buchi Pure C-810 纯化分离系统
BUCHI Rotavapor R-300
真空恒温干燥箱
保干器
高效液相色谱
2.2 试剂及耗材
色谱柱 4g
1mL 一次性塑料注射器
500mL 圆底烧瓶
研钵
试剂(分析纯): 甲醇、水
2.3 样品和准备工作
样品:正相柱层析的组分 G-12
将 G-12 保干后称重得质量 m=2.5775g,将该组分全部溶于甲醇(分析级)后倒入研钵中,加入该组分质量 0.8 倍的 C-18 填料拌样,拌干后装入柱子中,又下至上按照 C-18 硅胶、样品、保护硅胶填满整根柱子。
2.4 实验过程
极性组分分离过程包括快速分离制备色谱柱的活化、极性组分的分离、浓缩和称重。
2.4.1 色谱柱的活化
取一支色谱柱 4g 安装在 Pure C-810 上,连接好溶剂、管路, 按照 表1 参数平衡色谱柱,充分活化。
表 1:色谱柱平衡参数
Equilibration time | 10min | |
Flow rate | 15mL/min | |
Methanol % | 20 | |
Water % | 80 | |
表 2:极性组分分离参数及洗脱梯度
参数表 | ||
Solvent A | Methanol | |
Solvent B | Water | |
Flow rate | 15mL/min | |
UV length 1 | 254nm | |
UV length 2 | 210nm | |
UV length 3 | 280nm | |
UV length 4 | 320nm | |
UV sensitivity | low | |
UV threshold | 0.05AU | |
Collection | No Collection | |
梯度表 | ||
Time/min | Solvent | %2nd |
0 | AB | 80 |
25 | AB | 80 |
0 | AB | 60 |
35 | AB | 60 |
0 | AB | 40 |
50 | AB | 40 |
0 | AB | 30 |
80 | AB | 30 |
0 | AB | 20 |
70 | AB | 20 |
0 | AB | 10 |
54 | AB | 10 |
0 | AB | 0 |
60 | AB | 0 |
2.4.2 极性组分的收集与浓缩
以 500mL 收集瓶为收集容器外置在一侧,从洗脱开始收集洗脱液。如 图2 所示:

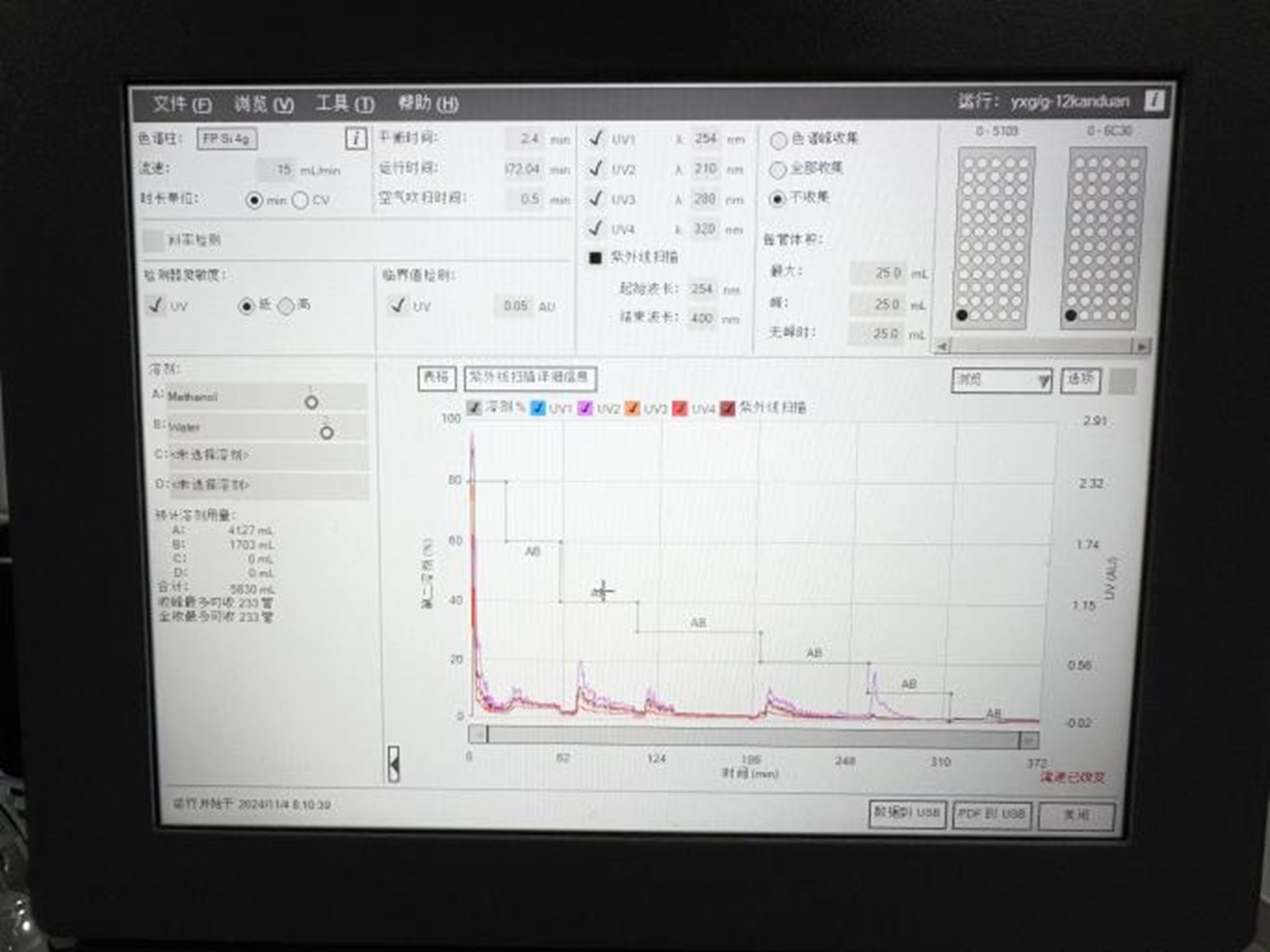
▲ 图2:安装色谱柱,极性组分洗脱液的收集及操作界面
取干净的 500mL 圆底烧瓶烘干,根据色谱分离图谱将收集到的极性洗脱液转入烧瓶中,旋蒸除去溶剂,将样品转移至西林瓶中,按照相同步骤收集浓缩相应极性组分,将所有组分吹干后放入保干器中干燥24h后称重。实验进行过程中,通过紫外检测器我们可以观察到样品的出峰情况,可以根据此情况调整洗脱时间,尽可能的提高效率。
3
结果
3.1 G-12 的极性组分分离图谱
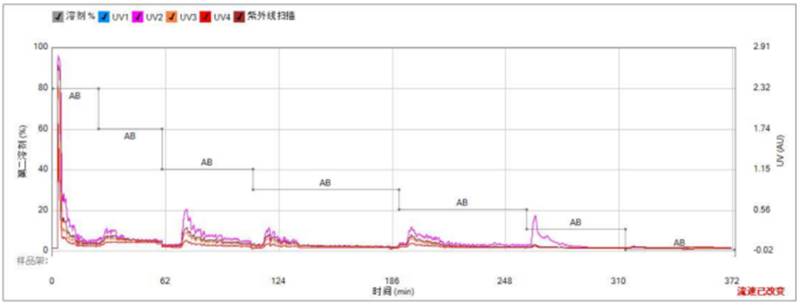
▲ 图 3:G-12 极性组分分离图谱
3.2 G-12 极性组分含量
样品名称 | m [mg] | |
G-12-1 | 1211.8 | |
G-12-2 | 108.8 | |
G-12-3 | 196.3 | |
G-12-4 | 248.0 | |
G-12-5 | 380.3 | |
G-12-6 | 139.8 | |
G-12-7 | 42.1 | |
各极性组分质量和与 G-12 样品质量相比并未有太大差距,证明利用此法样品损耗量小。
3.3 分离效果高效液相色谱验证
将浓缩后的组分溶于适量色谱甲醇中,高效液相色谱分析条件为 20-95 甲醇 25min,100甲醇 10min,分离效果如 图5 所示,结果表明各极性组分分离效果良好,并且将前 5min 的大峰单独分离出来后,后 20min 的小峰均显现出来,有助于分离单体化合物。
图 5:极性组分高效液相色谱图
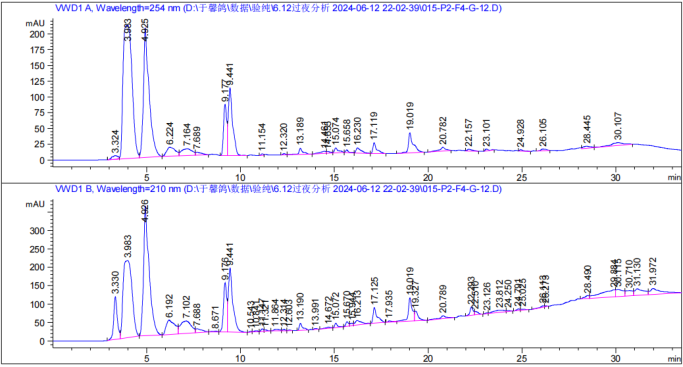
▲ G-12 组分分析图
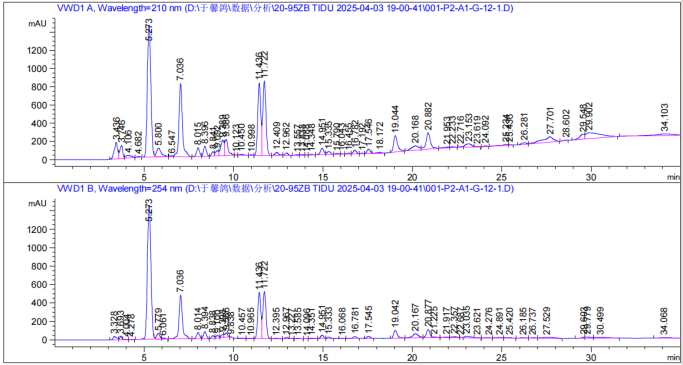
▲ G-12-1 组分分析图(20%甲醇)
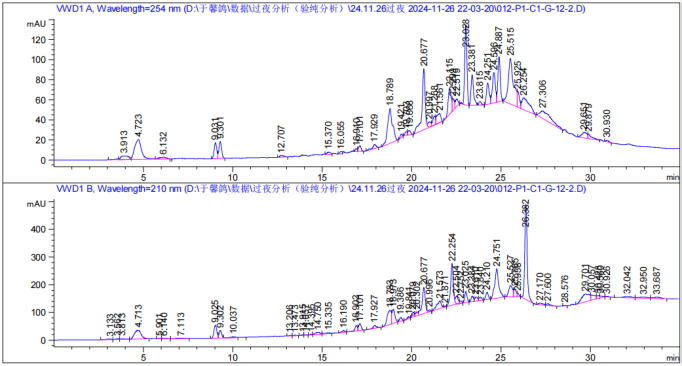
▲ G-12-2 组分分析图(40%甲醇)
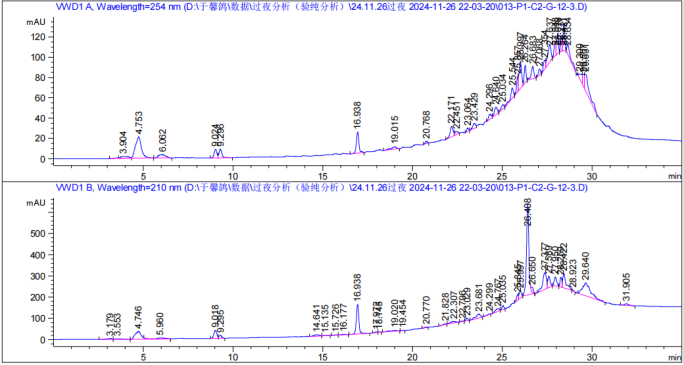
▲ G-12-3 组分分析图(60%甲醇)
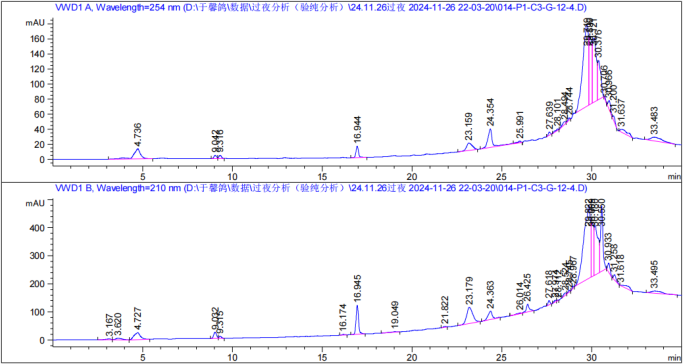
▲ G-12-4 组分分析图(70%甲醇)
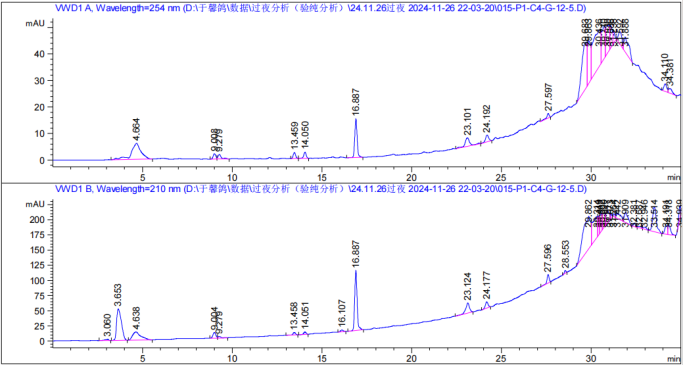
▲ G-12-5 组分分析图(80%甲醇)
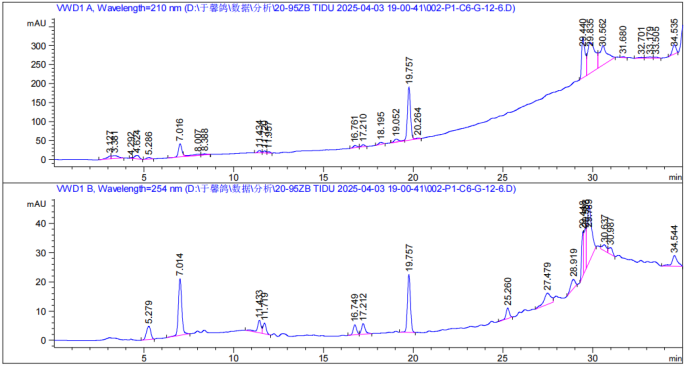
▲ G-12-6 组分分析图(90%甲醇)
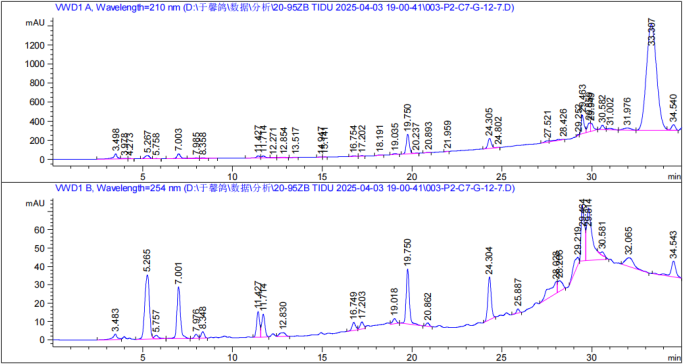
▲ G-12-7 组分分析图(100%甲醇)
4
结论
本应用用 BUCHI 制备型色谱仪 Pure C-810 对微生物次级代谢产物正相柱层析组分按极性进行分离,分离色谱图表明该组分分离效果良好,组分损耗较少,且通过高效液相色谱验证,许多原本看不到的小峰在进行砍段后可以显现,证明此法的可行性。
5
参考文献
Operation manual of Pure C-810

长按上方二维码联系我们
或拨打联系电话:
400 - 880 - 8720