

根据不同标准方法
测定硫酸盐灰分
灰分测定
硫酸盐灰分测定是药品质量控制中评价药品成分纯度和质量的一项重要分析技术。硫酸盐灰分的测定包括加入硫酸,然后焚烧样品,去除所有的有机物,然后测定残留物。所得的残留物主要由无机盐组成,可以对其进行分析,得到有关杂质存在和样品质量的信息。硫酸盐灰分的测定是评价原料药质量的一个重要参数,关系到最终产品的有效性和安全性。药物中杂质的存在和无机阳离子的水平会影响最终产品的药效和纯度,在某些情况下,会对患者身体健康产生不利影响。因此,需要准确可靠的硫酸盐灰分测定方法,以保证药品的质量和安全。
1
介绍
各种药典方法已被开发用于测定药用物质中的硫酸盐灰分,包括美国药典(USP)、欧洲药典(EP)和中国药典(CP)方法。这些方法已在各地的药品质量控制实验室得到验证和广泛应用。然而,由于其中一些测定的复杂性和成本控制等,需要建立一种更简单、更经济、更准确的硫酸盐灰分测定方法。
本研究在 USP 药典方法的基础上,建立了一种简单、准确、安全、可靠的测定原料药中硫酸灰分的方法。该方法具有良好的准确性、安全性和优异的高温性能,同时也适用于阿司匹林等药用物质中硫酸灰分的测定。所得结果与预期结果吻合较好。该仪器可用于药品质量控制实验室的常规分析,为评价药品成分的纯度和质量提供了可靠的工具。
2
硫酸盐灰分测定
中国药典中对该硫酸灰分测定的方法为 0841 炽灼残渣检查法。
具体方法:
取供试品 1.0~2.0g 或各品种项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全炭化,放冷;除另有规定外,加硫酸 0.5~1ml 使湿润,低温加热至硫酸蒸汽除尽后,在 700~800℃ 炽灼使完全灰化,移置干燥器内,放冷,精密称定后,再在 700~800℃ 炽灼至恒重,即得。如需将残渣留作重金属检查,则炽灼温度必须控制在 500~600℃。
根据对比不同国家药典的方法研究,USP 和 EP 可以说完全一样,只是叫法不一样,与 CP 的区别为:
USP、EP 对加样品之前的坩埚不需要恒重,CP 要求加样品之前坩埚恒重。
USP、EP 对整个炽灼过程中要求不能产生火焰,CP 没要求。
USP、EP 判断结果是从首次完全炽灼后开始,如不超限度,判定合格,不需要再恒重;如超限度,需要循环最后一步,若在恒重前不超限度,判定合格,若直至恒重仍不合格,判定不合格。
温度要求不一样。

湿法消解仪 B-440

尾气吸收仪 K-415
湿法灰化系统由湿法消解仪 B-440 和尾气吸收仪 K-415 组成(如上图1),可以根据药品质量控制中的不同具体方法的选择可能取决于分析的目的、每天的样品量以及遵守官方标准方法的需要,轻松有效地进行灰化实验。
此外,它可用于不同药典的各种应用(温度高达600°C):
2302 灰分测定法
原子吸收光谱法或ICP进行元素分析前处理
镉和铅分析的预处理
Residue on ignition (USP 281)
Heavy metal test method (USP 231, Method II)
Loss on ignition test method (USP 733)
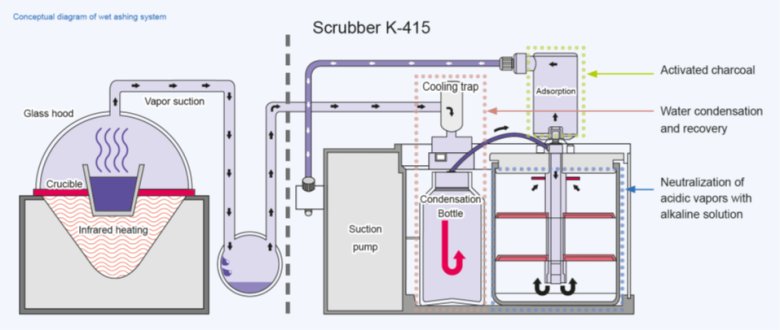
▲ 图 2. 湿法灰化系统示意图,由湿法消解仪B-440(左)和尾气吸收仪K-415(右)组成。
湿法消解仪 B-440 将样品加热到高达 600°C 的温度,尾气吸收仪提供多步骤进行吸收,以确保完全中和吸收灰化过程中产生的有害烟雾。
提供以下三个步骤:
预冷凝含水烟雾的冷凝阶段
用碱性溶液中和酸雾的中和阶段
活性炭对残留烟雾的吸附阶段
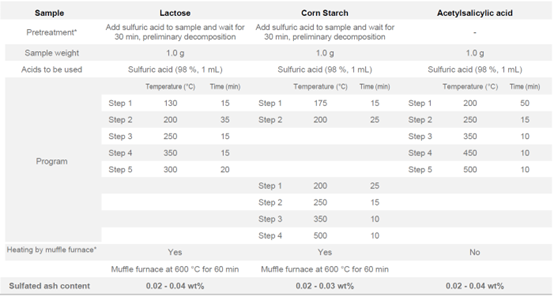
湿法灰化系统通过两种仪器的完美同步工作,得到最准确的结果。在这项研究中,通过对一些样品测试,如乳糖,玉米淀粉以及阿司匹林等。通过应用这些方法,测定的硫酸盐灰分含量低至 0.02 - 0.04 wt% (如表1),很好的吻合于样品的真值。
表1:测定不同样品的仪器参数及数据结果
3
结论
在这项研究中,我们提出了一种有效的方法,用于测定药用物质中的硫酸盐灰分。该方法在药典方法的基础上取得了良好的结果,证明了其作为药物质量控制实验室常规分析的可靠方法的潜力。使用湿法灰化系统,提高分析速度,精度和安全性。同时开发可靠的方法对于维持药品生产的高质量标准和确保患者安全至关重要。

长按上方二维码联系我们
或拨打联系电话:
400 - 880 - 8720
微信公众号
步琦智慧实验室
淘宝官方旗舰店
瑞士步琦