 白金会员
白金会员
 已认证
已认证
miRNA是一类由细胞的内源基因编码的长度约为22个核苷酸的非编码单链RNA分子,在细胞中发挥调控作用。癌细胞独特的胞内环境可以通过miRNA等生物标志物反映在其外泌体中。癌细胞来源的外泌体miRNA在癌症生物学中发挥着关键作用,可以作为癌症诊断的潜在生物标志物。然而,外泌体中miRNA的水平非常低。因此,以一种易于操作的方式识别、检测和量化疾病相关外泌体miRNA仍然存在挑战。

在上图中的这项最新研究中,研究团队开发出一种新方法来检测微量的癌症相关的外泌体miRNA。该检测方法基于CRISPR-Cas13a系统,该系统具有独特的RNA酶活性,而且灵敏、可靠和有效。研究团队先设计了一个CRISPR-Cas13a系统来切割荧光基团和淬灭剂标记的报告分子,然后将其包装到脂质体中,这一脂质体相当于人造版外泌体,再使用脂质体介导的膜融合(MFS)策略,将CRISPR-Cas13a系统转染到外泌体中。由于Cas13a具有独特的RNA酶(RNase)活性,RNA引导下Cas13a的反式切割活性可以裂解荧光团和淬灭剂标记的报告细胞,导致靶标RNA触发RNA酶激活后荧光增强。当脂质体和外泌体融合在一起时,如果外泌体中存在靶标miRNA序列,CRISPR-Cas13a就会识别并结合到靶标miRNA,然后激活反式切割活性,有效切割并产生放大的荧光信号。
上图展示了乳腺癌细胞(MCF-7)来源的外泌体与健康人乳腺上皮细胞(MCF-10A)来源的外泌体以不同比例混合后,在ZetaView散射光检测模式和荧光检测模式下的检测情况: A图:散射光模式下,尽管不同样品的混合比例不同,但ZetaView能检测的外泌体颗粒数量比较接近;荧光模式下,随着含miR-21核酸的癌细胞外泌体比例降低,ZetaView检测到的荧光颗粒明显减少。 B图:ZetaView散射光模式下测到的外泌体颗粒总浓度比较接近。 C图:ZetaView荧光模式下测到的荧光颗粒浓度随着癌细胞外泌体比例降低而明显降低。 从该临床样本的荧光检测结果来看,乳腺癌患者与健康捐赠者的miR-21表达差异显著。 研究团队表示,基于CRISPR-Cas13a的MFS-CRISPR平台,可以直接用于检测血液样本,并成功区分来自乳腺癌患者和健康捐赠者的临床样本。因此,通过MFS-CRISPR平台检测分析血液样本,有望实现更快、更简便的癌症诊断和监测。 张俊利,师从张振中教授,于2021年12月入职于郑州大学药学院,直聘副研究员,主要研究方向为生物标志物分析。相关研究成果以作者或通讯作者在Journal of Extracellular Vesicles(2020,IF:25.841)、ACS Sensors(2023, IF:9.618)、Analytical Chemistry(2023, IF:8.008)、ACS Applied Materials & Interfaces(2020, IF:9.229)、Nanoscale(2022, IF:8.307)、Sensors and Actuators B:Chemical(2018, IF:6.393)和ACS Biomaterials Science & Engineering(2021, IF:5.395)等期刊上发表SCI论文7篇,授权国家发明专利1项。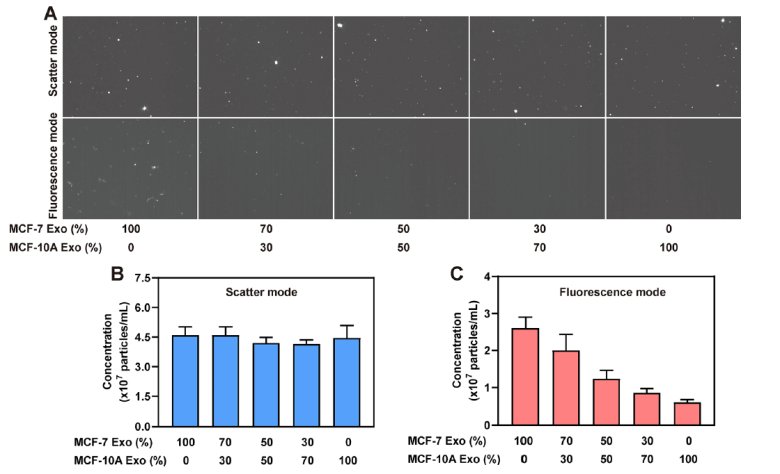
△ 作为目前最新款的NTA产品,ZetaView不仅能实现传统NTA技术对纳米颗粒粒径和浓度的表征,还能测定样品在特定条件下的Zeta电位,为样品稳定性和表面修饰结果提供可靠的数据支持。在荧光标记实验中,ZetaView不仅能实现传统NTA技术对某个标志物的表征,还能通过配备双激光或四激光,在单次进样中,同时完成多个标志物的鉴定,并提供可靠的共定位(Colocalization)检测结果,帮助用户更全面地了解标志物表达情况,助力用户深度挖掘更多的标志物信息。 相比于传统的NTA产品,ZetaView不仅功能更全面,其操作和维护也更加简单方便。它可以实现自动清洗、自动校准,样品池无需拆卸,即可完成快速清洗。这些特点都在更大程度地帮助用户减少操作时间、提高实验效率,加速用户的研究进度。ZetaView也因此而备受用户的青睐。



